食料品の塩分表示には「ナトリウム量表記」と「食塩相当量表記」の2種類があります。
この2種類の表記は本質的には同じで、ナトリウム量は食塩相当量に換算できます。
減塩中の方はナトリウム量の食塩相当量への換算方法は覚えておく必要があります。
なぜなら、ナトリウム量表記の食品を見たときに塩分で何gか分からなくなってしまうからです。
そこで、今回は簡単にナトリウム量を食塩相当量に換算する方法を解説します。
算数さえできれば誰でも簡単にナトリウム量をみて「これは食塩相当量〜g分だな」と計算できるようになります。
塩分制限中の方は是非読んで見てください。
また、後半ではナトリウムを食塩相当量に換算する方法の導出方法も解説します。
「なぜこの方法で換算できるの?」と気になる方は是非読んでみてください。
目次
【ナトリウム400mgで塩分1g】ナトリウム量と食塩相当量の換算方法

一般的に減塩目標は「食塩相当量で○g」といったように、食塩相当量に換算して減塩目標をたてます。
そのため「ナトリウム量」を「食塩相当量」の値に換算する必要があります。
そこで今回は、簡単にナトリウム量を食塩相当量に換算する方法を説明いたします。
重要な式はこれだけ!
つまり、ナトリウム400mgで食塩約1gです。
上記の式は、ある程度ざっくり計算するための式になります。
また、パッと400で割るのが難しいと言う方は次の計算方法がおすすめです。
(「2で割って、2で割って、100で割る」と声に出して覚えましょう)
ナトリウム量がかなり大きな値でも、半分にする(つまり、「2で割る」)のはとても簡単です。
また、100で割ると言う行為も桁を2つ小さくするだけなので簡単なはずです。
覚える際は「2で割って、2で割って、100で割る」と声に出して5回言って見て下さい。
簡単に覚えることができますよ。
「換算方法だけ知れればいい」という方はここまで読めば大丈夫です。
しかし、
「塩分とナトリウムって何が違うの?」
「換算式ってどうやって導出されたの?」
ということが気になる方は、是非続きも読んでみてください。
「食塩相当量」と「ナトリウム」の違い
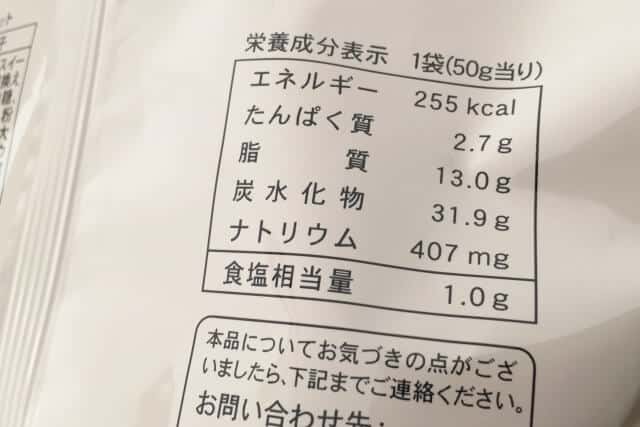
食料品の塩分表示を見ると「ナトリウム量」と書いてあるものを、「食塩相当量」と書いてあるものがあります。
それでは、この「ナトリウム量」と「食塩相当量」は何が違うのか解説します。
結論を先にお話ししますと、
「ナトリウム量」 = 「食塩に含まれるナトリウム」+「食材由来のナトリウム」
つまり、食塩相当量とは、食品に含まれる全てのナトリウム量を食塩に換算した量なのです。
それでは、「食塩相当量」と「ナトリウム量」の違いを解説するために順を追って以下の2点を解説します。
・「食塩とは」
・「ナトリウムは食塩以外にも含まれる」
それでは、なぜ換算できるのかを解説します。
【NaCl】食塩とは
ここで、「食塩とは」というお話をします。
「食塩」とは専門的な言い方をすると「塩化ナトリウム」のこと。
「塩化ナトリウム」は化学式では「NaCl」と記述されます。
つまり、食塩は「Na(ナトリウム)」と「Cl(塩素)」という2つの原子でできいるのです。
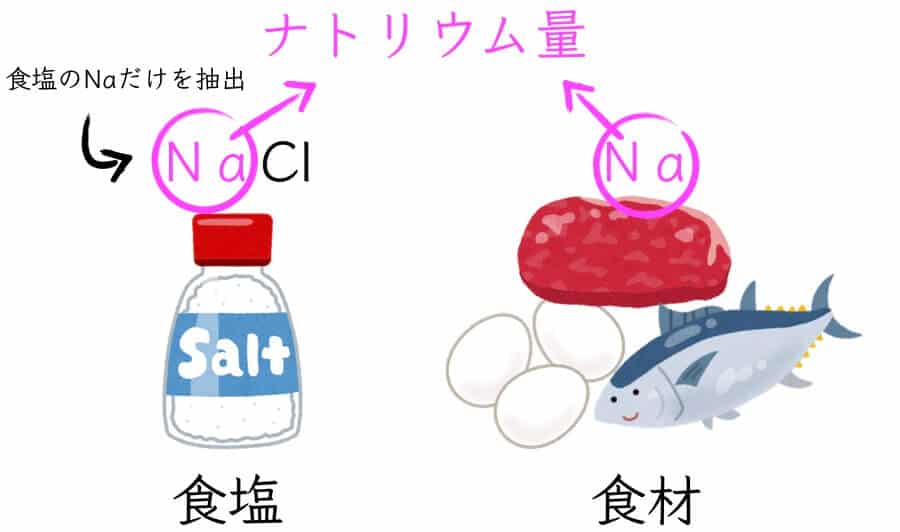
ここまでお話しすればわかると思いますが、つまりナトリウム量とは「ナトリウム(Na)」の量のことです。
しかし、ナトリウムは食塩(NaCl)以外にも含まれており、ナトリウム量はその全てのナトリウムを合計した値です。
ナトリウムは食塩以外にも含まれる
「食塩=Na + Cl」と話しましたが、食品には食塩由来以外にも微量に素材由来のナトリウムが含まれます。
この本来食塩ではない素材由来の単体のナトリウムまでもを「食塩(NaにClを加えた物質)だったら何gになるのか?」と換算した値が食塩相当量です。
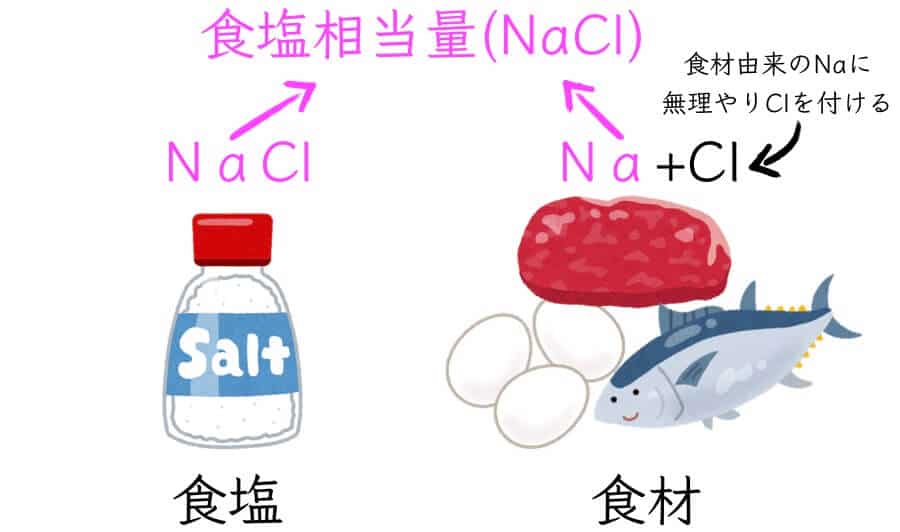
「ナトリウム量」 = 「食塩に含まれるナトリウム」+「食材由来のナトリウム」
食塩相当量は、「ナトリウム量」の全てのNaに塩素(Cl)がくっついて塩化ナトリウム(NaCl)になったと仮定したときのNaClの量。
換算式の導出方法
さて、次は換算式の導出方法を説明します。
気になる方だけ見ていただければ大丈夫です。
NaとClの原子量(原子の重さの基準)はそれぞれ次の通りです。
単位は[g/mol]ですが、わからない方は単位は無視していただいて大丈夫です。(高校1年の化学で習います)
原子量について、誤解を恐れず説明させてもらうと「原子量とはNaとClの重さの比」のことです。
つまり、Naが1個で22.99gあると仮定したとき、Clは1個で35.45gある、と言うこと。
※厳密には「1個で」と言うのは変な言い方なのですが、説明を易しくするためにそうしておきます。
ここで、食塩=NaClでした。
NaClはNa+Clなので
NaCl(食塩) = 22.99 + 35.45 = 59.44
ナトリウム 塩素
ここで、食塩にナトリウムが重さで何%含まれているか計算します。
Na / NaCl = 22.99 ÷ 59.44 ≅ 40%
つまり、NaClの中には重さで約40%のNaが含まれていることになります。
わかりやすくて言い換えると、
食塩(NaCl)が10gあるとき、4gはNaで6gはClと言うことです。
また一般的に食品の栄養表示では、ナトリウムは[mg]と言う単位で計算されます。
一方で、食塩相当量は[g]と言う単位で計算されます。
mgとgの関係は、1g=1000mgといった関係です。
そのため、gを1000倍すればmgに換算できます。
メートル(m)をミリメートル(mm)に直すには1000倍しますよね。
以上、導出のポイント①、②より以下の式が導かれます。
食塩相当量[g] × 40% × 1000 = ナトリウム量[mg]
次に、40%は数字に直すと0.4なので、左辺の数字は0.4×1000 = 400となります。
食塩相当量[g] × 400 = ナトリウム量[mg]
さらに、両辺を400で割ると
食塩相当量[g] = ナトリウム量[mg] / 400
この記事の冒頭で紹介した、ナトリウムを食塩相当量に換算する式が導出ができました。
この記事はここで以上になります。
お役に立ちましたら、SNS共有・ブックマークなどお願します。
楽しく、正しく減塩していきましょう!
参考:KYOWA KIRIN